胶东在线11月17日讯 美国时间11月15日,加州圣地亚哥,美国风湿病学会(ACR,American College of Rheumatology)2023年会现场,荣昌生物制药(烟台)股份有限公司(688331.SH/9995.HK)受邀以口头报告的形式,正式宣布全球首款BLyS/APRIL抑制剂泰它西普(Telitacicept,商品名:泰爱®)治疗类风湿性关节炎(RA)患者的Ⅲ期临床试验,达到所有主要终点并显示出良好的安全性。目前,国家药品监督管理局药品审评中心(CDE)已受理泰它西普治疗类风湿关节炎的新药上市申请。

荣昌生物高级副总裁、自身免疫性疾病全球临床开发主管Qing Zuraw博士在ACR年会现场作口头报告
美国风湿病学会(ACR)是全球规模最大、最负盛名的风湿学会议。一年一度的ACR年会汇聚了最新的研究成果和最具影响力的演讲嘉宾,已成为医学人士获取最前沿风湿病学研究与临床应用信息的重要平台。

2023ACR年会现场的荣昌生物展区
此次ACR年会报告的泰它西普类风湿关节炎Ⅲ期临床试验,是一项随机、双盲、安慰剂对照、多中心的Ⅲ期临床研究,旨在评估160mg泰它西普与安慰剂在对甲氨蝶呤(MTX)反应不足的RA患者中的疗效和安全性。研究共入组479例类风湿关节炎患者,主要疗效终点是在第24周达到ACR20应答的患者比例。次要疗效终点包括ACR50和ACR70应答率,ACR应答的各个组成部分,DAS28-ESR以及在第24周通过mTSS测量的放射学关节损伤。
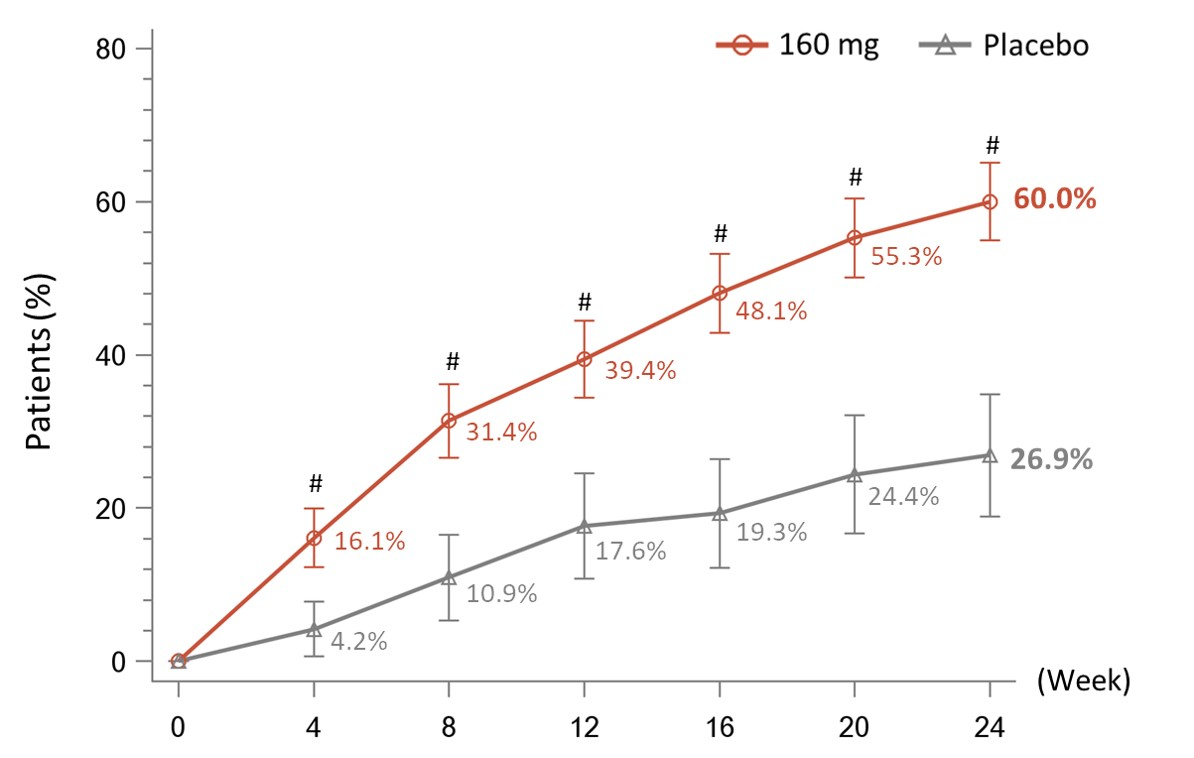
两治疗组的ACR20应答率随时间的变化
数据显示,此项Ⅲ期临床试验达到主要临床终点和次要终点。研究结果证明了泰它西普在治疗对MTX反应不足的中重度类风湿关节炎患者的疗效和安全性。
数据显示,24周时,与安慰剂组相比,泰它西普组ACR20应答率显著增加(60.0% vs 26.9%,P<0.001)。在第24周,泰它西普组的ACR50应答率显著高于安慰剂组(21.4%vs.5.9%,P<0.001),并且在DAS28-ESR较基线降低以及ACR应答标准的各个组成部分方面,均显著优于安慰剂组。此外,泰它西普组在第24周无放射性学进展(△mTSS≤0)的患者比例显著高于安慰剂组(90.2% vs 66.4%,P<0.001)。与基线相比,泰它西普组的患者关节损伤进展(根据mTSS、关节间隙狭窄评分和侵蚀评分)在第24周时显著减少。
安全性方面,泰它西普组与安慰剂组在治疗相关不良事件(TEAEs)、严重不良事件(SAEs)、导致停止研究治疗的TEAEs以及感染发生率方面相似。研究期间未见死亡事件。
类风湿关节炎(RA)是一种慢性自身免疫性疾病,以侵蚀性关节炎为主要特征,发病初期的关节表现为关节晨僵、肿胀、疼痛等,最后可发生关节畸形并丧失关节正常功能,严重影响患者生活质量。根据弗若斯特沙利文报告,全球类风湿关节炎患者发病人数预计将于2025 年达到 4,220 万人(包括中国 620 万人),并于 2030 年达到 4,500 万人(包括中国 640 万人)。当前类风湿关节炎的标准治疗以抗炎类、糖皮质激素、传统免疫抑制剂及TNF-α抑制剂等药物为主,对于上述疗法无效或不耐受的患者而言,存在尚未满足的临床需求。
泰它西普是由公司CEO、首席科学官房健民教授发明设计的一个抗体融合蛋白药物分子,通过同时抑制BLyS和APRIL两个细胞因子的过度表达,“双管齐下”阻止B细胞的异常分化和成熟,从而治疗B细胞介导的系统性红斑狼疮等一系列自身免疫性疾病。2021年3月9日,泰它西普系统性红斑狼疮适应症正式获得国家药监局的国内上市批准,同年底进入国家医保药品目录。除系统性红斑狼疮适应症外,泰它西普治疗IgA肾炎、原发性干燥综合征、视神经脊髓炎谱系疾病、重症肌无力等适应症的Ⅲ期临床研究也在推进中。

 世界无烟日丨吸烟对身体的危害 一定要知道
世界无烟日丨吸烟对身体的危害 一定要知道 图解丨谈“癌”色变?带你正确认识肺癌
图解丨谈“癌”色变?带你正确认识肺癌